EMA vydala podmíněné schválení vakcíně Nuvaxovid (Novavax) pro osoby 18+ užívané ve dvou dávkách 21 dnů od sebe.
ema.europa.eu/en/news/ema-re…
ema.europa.eu/en/news/ema-re…

Na webu EMA již je zveřejněna podrobná veřejná hodnotící zpráva (EPAR) a my se podíváme trochu kriticky pod pokličku 👇ema.europa.eu/en/documents/a…
PRODUKT:
💉Proteinová vakcína, která obsahuje S-protein (původní wu-han varianty) a saponinový adjuvant Matrix-M pro lepší imunitní reakci.
💉Složení, viz obrázek
💉Proteinová vakcína, která obsahuje S-protein (původní wu-han varianty) a saponinový adjuvant Matrix-M pro lepší imunitní reakci.
💉Složení, viz obrázek

Preklinika (studie na zvířatech).
🧐Mně osobně chybí studie biodistribuce značené vakcíny, abychom věděli, kam se po vpíchnutí dostane nejvíce proteinu a kde zůstává (studie bude). Jinak za mě asi nic zvláštního/alarmujícího.


🧐Mně osobně chybí studie biodistribuce značené vakcíny, abychom věděli, kam se po vpíchnutí dostane nejvíce proteinu a kde zůstává (studie bude). Jinak za mě asi nic zvláštního/alarmujícího.



KLINIKA (to důležité)
💉Podkladem byly 4 studie, jako hlavní (pivotal) byly studie 301 a 302 (placebem kontrolované, dvojitě zaslepené, RCT)
💉Mechanismus této vakcíny je tedy předložení plného (full-length) stabilizovaného S-proteinu (Wuhan) spolu se saponinovým adjuvantem

💉Podkladem byly 4 studie, jako hlavní (pivotal) byly studie 301 a 302 (placebem kontrolované, dvojitě zaslepené, RCT)
💉Mechanismus této vakcíny je tedy předložení plného (full-length) stabilizovaného S-proteinu (Wuhan) spolu se saponinovým adjuvantem


🧐Imunogenicita (hladiny protilátek) - mně osobně tenhle parametr mnoho neříká (když neznáme korelaci s klinikou), ale nechť:
💉Máme data po dobu 5 měsíců po 2. dávce a je pozorované snížení hladin protilátek - jestli to bude vyžadovat booster nebylo známo
💉Máme data po dobu 5 měsíců po 2. dávce a je pozorované snížení hladin protilátek - jestli to bude vyžadovat booster nebylo známo

💉Ve studii 302 byla snížená (1,5x) imunitní odpověď u pacientů, kteří obdrželi společnou vakcínu proti sezónní chřipce, ale klinický význam (nákazy, závažnost...) není zřejmý - z mechanismu by interakce neměla být, možná to je stářím těchto konkrétních účastníků. 

Z imunitního hlediska není známá potřeba 3 (booster dávky), význam hladin protilátek na klinické výsledky (correlate of protection) a schopnost neutralizace variant viru. 

KLINICKÁ ÚČINNOST
🧐hlavní studie jsou 301 a 302 a na ty se zaměříme specificky.
💉studie u 18+ (18-84), KTEŘÍ NEMĚLI PŘEDCHOZÍ PRODĚLANOU INFEKCI ‼️ 🧐takováto skupina již dnes asi není úplně "standardní"
💉Obě studie se zaměřovaly spíše na rizikové pacienty‼️🧐přenositelnost?
🧐hlavní studie jsou 301 a 302 a na ty se zaměříme specificky.
💉studie u 18+ (18-84), KTEŘÍ NEMĚLI PŘEDCHOZÍ PRODĚLANOU INFEKCI ‼️ 🧐takováto skupina již dnes asi není úplně "standardní"
💉Obě studie se zaměřovaly spíše na rizikové pacienty‼️🧐přenositelnost?

🧐V těchto dvou studiích byly použity lehce jiné produkty oproti tomu, co byl nakonec schválen - ten je víc podobný tomu ve studii 301. (to je detail, který se dá vyřešit tím, že výrobce pak prokazuje podobnost produktu...) 

💉PRIMÁRNÍ PARAMETR: snížení rizika PCR+ symptomatické infekce od 7. dne po 2. dávce (interval 21 dnů)
🧐Ve studii 302 si to ještě vymezili u serologicky negativních dospělých

🧐Ve studii 302 si to ještě vymezili u serologicky negativních dospělých


🧐Ve studii 301 došlo k ukončení náboru účastníků (kvůli snížení prevalence a nouzovému schválení jiných vakcín v USA v květnu 2021). Všichni účastníci byli tedy zaslepeně převedeni na rameno vakcíny ‼️ a byla pouze vyhotovena jedna analýza. 

🧐Obě studie měly poměrně vysoký podíl pacientů končících ve studii, vyšší v rameni placeba a docházelo často k odslepení (až 35%‼️) z důvodu toho, že se účastníci chtěli nechat očkovat již schválenými vakcínami. 




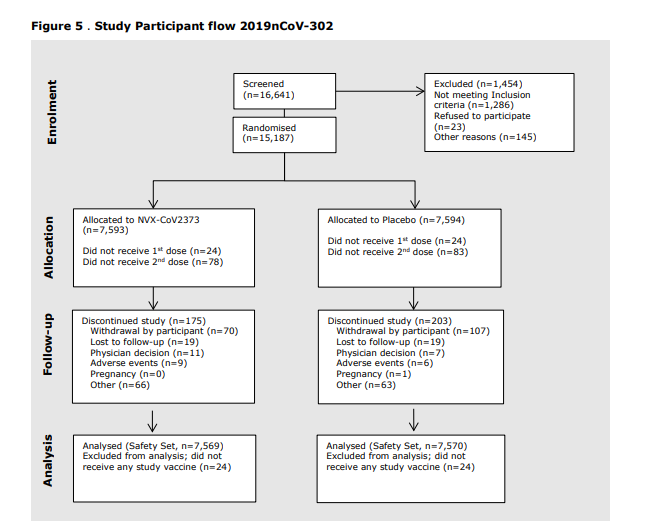


💉Drtivá většina účastníků předtím neprodělala covid (>90%) (🧐přenositelnost na prodělavší?)
💉Hodně z nich (až 95%) mělo nějaké rizikové faktory závažného průběhu (🧐přenositelnost na méně rizikové?)

💉Hodně z nich (až 95%) mělo nějaké rizikové faktory závažného průběhu (🧐přenositelnost na méně rizikové?)


⚠️PRIMÁRNÍ VÝSLEDKY
💉301: 14 sympt. případů u vakcíny, 63 (5 závažných, 3 hospitalizace) u placeba => účinnost 90,4%
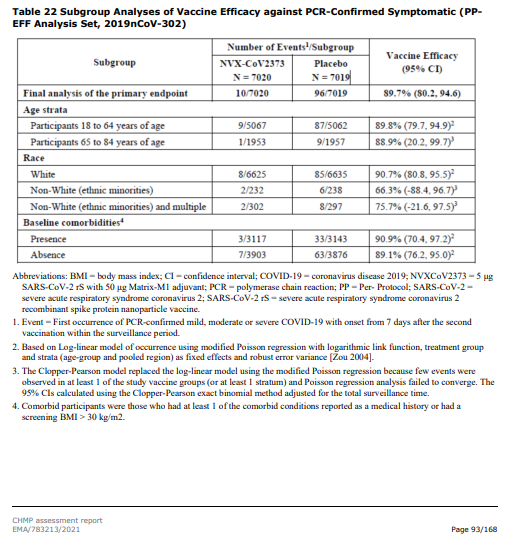
💉302: 10 případů u vakcíny, 96 (4 závažných, 1 hospitalizace) u placeba => účinnost 89,7%


💉301: 14 sympt. případů u vakcíny, 63 (5 závažných, 3 hospitalizace) u placeba => účinnost 90,4%
💉302: 10 případů u vakcíny, 96 (4 závažných, 1 hospitalizace) u placeba => účinnost 89,7%



🧐Z těchto studií se nedala vypočítat účinnost proti variantě delta (natož omicron)
🧐S ohledem na nízký počet případů není možné dobře vypočítat účinnost na snížení závažných/hospitalizací/úmrtí

🧐S ohledem na nízký počet případů není možné dobře vypočítat účinnost na snížení závažných/hospitalizací/úmrtí


🧐Nezamlouvá se mi nízká účinnost u podskupiny bez rizikových faktorů (bez komorbidit), ale je možné, že je to nízkým počtem účastníků (zejména u 301)... 


BEZPEČNOST
💉Většina nežádoucích příhod byla mírná, bolest, bolest hlavy, únava, atd. - nápadné je navýšení četnosti po 2. dávce.
💉Většina nežádoucích příhod byla mírná, bolest, bolest hlavy, únava, atd. - nápadné je navýšení četnosti po 2. dávce.

💉Vyskytuje se signál zvýšeného výskytu hypertenze po vakcíně.
💉Byla hlášena jedna myocarditida (nemůže být vyloučen virový původ) a blíž by se měly monitorovat cerebrovaskulární příhody.

💉Byla hlášena jedna myocarditida (nemůže být vyloučen virový původ) a blíž by se měly monitorovat cerebrovaskulární příhody.


🧐V obou studiích zemřelo (mírně) více účastníků v rameni vakcíny (2 vs 1 a 9 vs 5), žádné úmrtí však nebylo vyhodnoceno ve vztahu s vakcínou. 



⚠️Nejistoty/limitace ohledně příznivých efektů
💉Trvání účinnosti (hodnoceno max cca 90 dnů od 2. dávky)
💉Účinnost proti závažnému onemocnění a hospitalizacím
💉Účinnost u imunokompromitovaných
💉Účinnost proti variantám (delta, omicron)
💉Trvání účinnosti (hodnoceno max cca 90 dnů od 2. dávky)
💉Účinnost proti závažnému onemocnění a hospitalizacím
💉Účinnost u imunokompromitovaných
💉Účinnost proti variantám (delta, omicron)

⚠️Nejistoty/limitace ohledně bezpečnosti
💉Dlouhodobá bezpečnosti (medián sledování 3 měsíce)
💉Těhotenství
💉Dlouhodobá bezpečnosti (medián sledování 3 měsíce)
💉Těhotenství

🛑KONEC DOKUMENTU
Takže...schváleno máme. Aby to bylo také "užitečné", je potřeba znát účinnost proti delta,omicron; trvání ochrany případně boosteru, účinnost u lidí, kteří již prodělali a případně heterologní booster po předchozí jiné vakcíně.
Kupa práce, ale věřím, že probíhá.
Takže...schváleno máme. Aby to bylo také "užitečné", je potřeba znát účinnost proti delta,omicron; trvání ochrany případně boosteru, účinnost u lidí, kteří již prodělali a případně heterologní booster po předchozí jiné vakcíně.
Kupa práce, ale věřím, že probíhá.
Například dělají na boosteru a na omicron-specifické vakcíně: ir.novavax.com/2021-12-22-Nov…
Sice tam nemají klinická data, ale již mají preprint imunogenicity (hladiny protilátek) a bezpečnosti boosteru po 6 měsících versus 2 dávky. (to ale není zatím schválené)
medrxiv.org/content/10.110…
-neutralizují deltu a omicron
-po 3. dávce opět víc NÚ


medrxiv.org/content/10.110…
-neutralizují deltu a omicron
-po 3. dávce opět víc NÚ



@threadreaderapp please unroll
• • •
Missing some Tweet in this thread? You can try to
force a refresh