Welche unterschiedlichen Auswirkungen haben die verschiedenen #SARSCoV2-Varianten auf Zellen des zentralen Nervensystems und die Funktionen der Blut-Hirn-Schranke?
➡️ „Das Wildtyp-Virus und #Omicron haben höheres Potenzial für neurologische Schäden.“
#COVID19 #LongCovid #Corona
➡️ „Das Wildtyp-Virus und #Omicron haben höheres Potenzial für neurologische Schäden.“
#COVID19 #LongCovid #Corona

➡️ „Diese Ergebnisse deuten darauf hin, dass SARS-CoV-2 neurotrop ist, mit schädlichen Folgen für die Integrität der Blut-Hirn-Schranke (BHS) und die Zellen des Zentralnervensystems, die neurologischen Störungen nach einer SARS-CoV-2-Infektion zugrunde liegen könnten.“
Forscher am Francis Crick Institute (London) haben in Laborexperimenten gezeigt, dass Varianten von SARS-CoV-2 die Blut-Hirn-Schranke beeinträchtigen und Gehirnzellen auf unterschiedliche Weise schädigen können. Insgesamt deuten die Arbeiten darauf hin, dass SARS-CoV-2 die 

normalen physiologischen Funktionen der BHS und ihrer zellulären Komponenten beeinträchtigt und somit zu dem breiten Spektrum an neurologischen Manifestationen von SARS-CoV-2 beiträgt, die klinisch beobachtet worden sind. Genauer gesagt zeigen die Ergebnisse, dass das WT-Virus 

und die #Omicron-Variante aufgrund ihrer Fähigkeit, ZNS-Zellstress zu induzieren, die extrazelluläre Glutamatkonzentration zu beeinflussen und die zellulären Komponenten der BHS zu schädigen, ein höheres Potenzial für neurologische Schäden haben. 

Die Eta-, Delta-, Beta- und Alpha-Varianten scheinen vergleichsweise geringere Auswirkungen auf die neurologische Gesundheit zu haben, da sie entweder keinen direkten Zelltod verursachen, die Glutamatkonzentration nicht signifikant beeinflussen oder keinen Zusammenbruch der BHS 

hervorrufen. Die wichtigsten Theorien dazu wie das Virus in das Gehirn gelangen sind, dass es durch die Nerven, die den Geruchssinn übertragen, oder durch die Blut-Hirn-Schranke, eine selektive Barriere, die das Gehirn und den Blutkreislauf trennt, eindringt. In dieser Studie 

wurden Gehirnzellen und ein 3D-Modell einer Blut-Hirn-Schranke verschiedenen Stämmen von SARS-CoV-2 ausgesetzt: Wildtyp (die ursprüngliche Variante aus Wuhan), Alpha, Beta, Delta, Eta und Omicron. Bei den untersuchten Hirnzellen handelte es sich um Perizyten, Astrozyten, 

Endothelzellen und Mikroglia - Zellen, die Nervenzellen unterstützen und kontrollieren, wie durchlässig die Blut-Hirn-Schranke für Moleküle und Zellen ist.
Die Forscher wiesen nach, dass alle Varianten Stress für die Gehirnzellen verursachen und sie an ihrer Arbeit hindern, aber
Die Forscher wiesen nach, dass alle Varianten Stress für die Gehirnzellen verursachen und sie an ihrer Arbeit hindern, aber
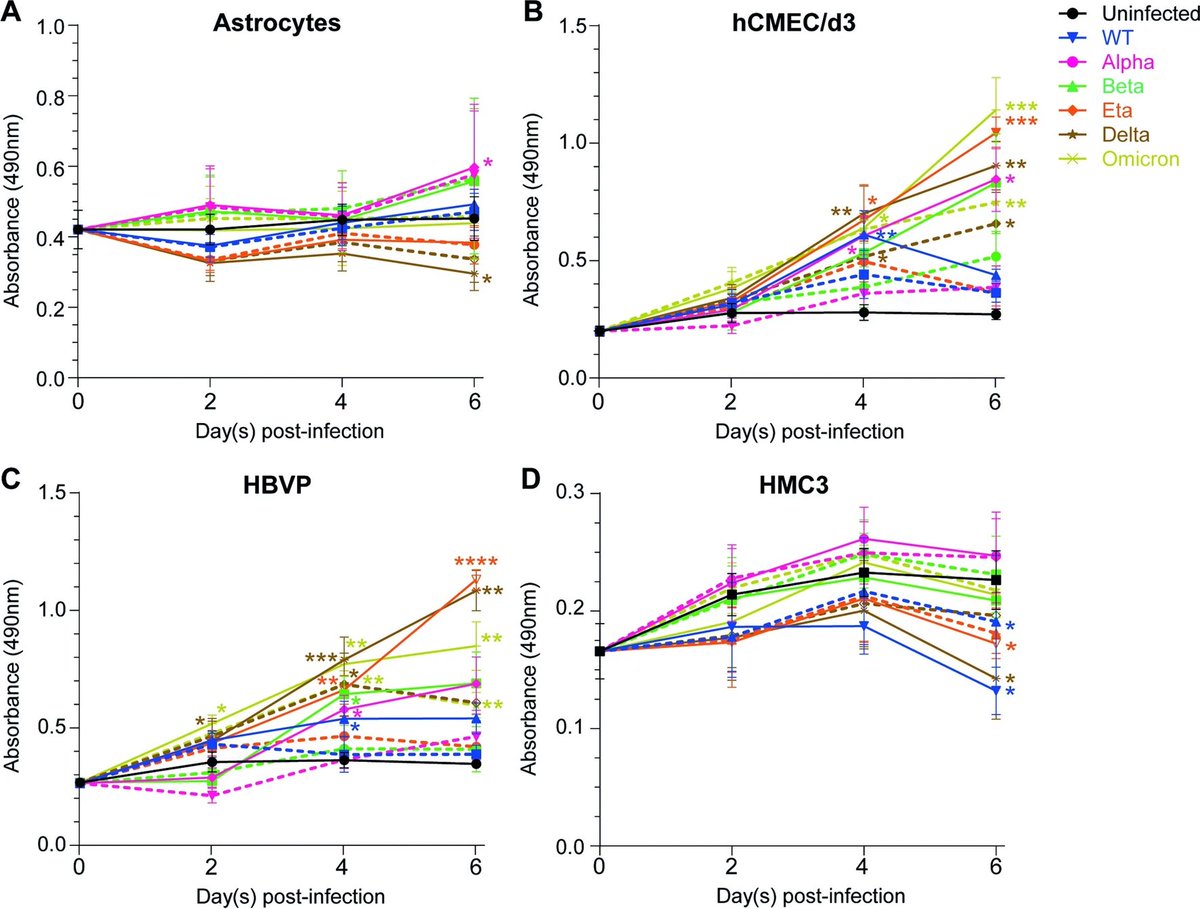
welche Zellen genau betroffen sind, hängt von der jeweiligen Variante ab. Das Wildtyp-Virus tötete alle Zelltypen außer Astrozyten, während Alpha und Beta nur Perizyten und Omicron Endothelzellen und Perizyten abtötete. Die Forscher untersuchten auch, wie gut die Varianten die 

Blut-Hirn-Schranke im Modell überwinden. Das Wildtyp-Virus und in geringerem Maße auch Omicron waren in der Lage, die Integrität der Schranke zu stören, während dies den anderen Varianten nicht gelang. Die Forscher vermuten, dass das Virus, das die Schranke beschädigt und ihre 
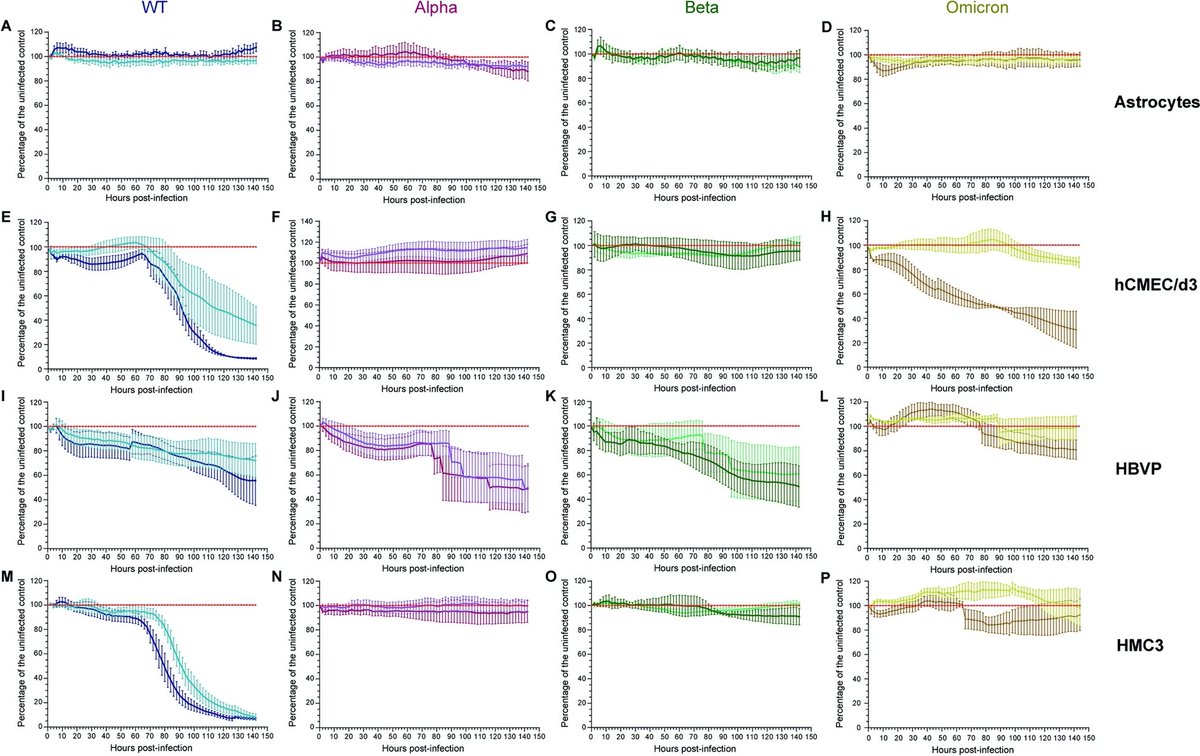
Durchlässigkeit erhöht, dazu führen könnte, dass Immunzellen in das Gehirn eindringen und eine Entzündung auslösen. Omicron tötete die Endothelzellen, die die Schranke auskleiden, aber es sah so aus, als bliebe die Durchlässigkeit der Blut-Hirn-Schranke intakter, was darauf 

hindeutet, dass die anderen Zellen in der Schranke zu ihrem Schutz beitragen könnten. Das Team stellte außerdem fest, dass alle Varianten mit Ausnahme der Eta-Variante die Verbindungsstellen an der Schranke negativ beeinflussten - Strukturen, die benachbarte Zellen miteinander 

verbinden und normalerweise verhindern, dass Moleküle zwischen den Zellen hindurchtreten -, was ebenfalls die Wirksamkeit der Schranke beeinflussen könnte. Die Forscher untersuchten auch, wie sich die Varianten auf die Konzentration von Glutamat auswirkten, einer Chemikalie im
Gehirn, die Nachrichten von Zelle zu Zelle überträgt. Die Glutamatmenge wird streng kontrolliert, da ein Zuviel oder Zuwenig schädlich ist. Die Untersuchung ergab, dass alle Varianten außer Beta die Glutamatmenge im Gehirn beeinflussten, indem sie sie entweder bis zu potenziell
toxischen Mengen erhöhten oder sie verringerten und damit die Fähigkeit der Zellen, Botschaften zu übermitteln, beeinträchtigten. Alize Proust, leitende Laborforscherin im Tuberkulose-Labor am Crick und Erstautorin, sagte: "Es gab viele Spekulationen darüber, wie COVID-19
neurologische Symptome verursacht, und ob dies indirekt über eine Entzündung geschieht, oder ob das Virus direkt Gehirnzellen angreifen oder die Barriere überwinden kann. Wir haben gezeigt, dass das Virus im Labor beides kann, aber die Auswirkungen sind variantenspezifisch.
"Dies hat Auswirkungen auf das, was wir bereits gesehen haben. Menschen können nach einer COVID-19-Infektion neurologische Störungen entwickeln, manchmal erst Monate später. Wenn das Virus also einige Gehirnzellen abtötet, könnte dies den Beginn einer Krankheit, die das Gehirn
betrifft, beschleunigen. Unsere Arbeit könnte für Kliniker wichtig sein, um zu verstehen, welche Art von Schaden eine Variante verursacht, und um nach spezifischen Behandlungen zu suchen."
➡️ Insgesamt deutet diese Arbeit darauf hin, dass SARS-CoV-2 die normalen physiologischen Funktionen der Blut-Hirn-Schranke und ihrer zellulären Komponenten beeinträchtigt und somit zu dem breiten Spektrum an neurologischen Manifestationen von SARS-CoV-2 beiträgt, die klinisch 

beobachtet worden sind. Insbesondere zeigen unsere Ergebnisse, dass das WT-Virus und die Omicron-Variante aufgrund ihrer Fähigkeit, ZNS-Zellstress auszulösen, die extrazelluläre Glutamatkonzentration zu beeinträchtigen und die zellulären Komponenten der BHS zu schädigen,
ein höheres Potenzial für neurologische Schäden haben könnten. Die Eta-, Delta-, Beta- und Alpha-Varianten scheinen vergleichsweise geringere Auswirkungen auf die neurologische Gesundheit zu haben, da sie entweder keinen direkten Zelltod verursachen, die Glutamatkonzentration 

nicht signifikant beeinflussen oder keinen Zusammenbruch der BHS hervorrufen. Diese Arbeit könnte die Grundlage für künftige Forschungen über die Auswirkungen des Virus auf das menschliche Gehirn bilden und darüber Aufschluss geben, ob eine Impfung vor den in dieser Studie 

beobachteten Auswirkungen schützt.
Die Links zu Bericht und Studie:
https://t.co/Wi8KMbe3YW
#COVID19 #LongCovid #Corona #SARSCoV2 #Omicron #MECFS #CovidIsNotOver #CleanAir #MaskUp #Ventilation #AirQuality #ProtectTheKids #LongCovidKidscrick.ac.uk/news/2023-08-0…
jneuroinflammation.biomedcentral.com/articles/10.11…
Die Links zu Bericht und Studie:
https://t.co/Wi8KMbe3YW
#COVID19 #LongCovid #Corona #SARSCoV2 #Omicron #MECFS #CovidIsNotOver #CleanAir #MaskUp #Ventilation #AirQuality #ProtectTheKids #LongCovidKidscrick.ac.uk/news/2023-08-0…
jneuroinflammation.biomedcentral.com/articles/10.11…
• • •
Missing some Tweet in this thread? You can try to
force a refresh

 Read on Twitter
Read on Twitter