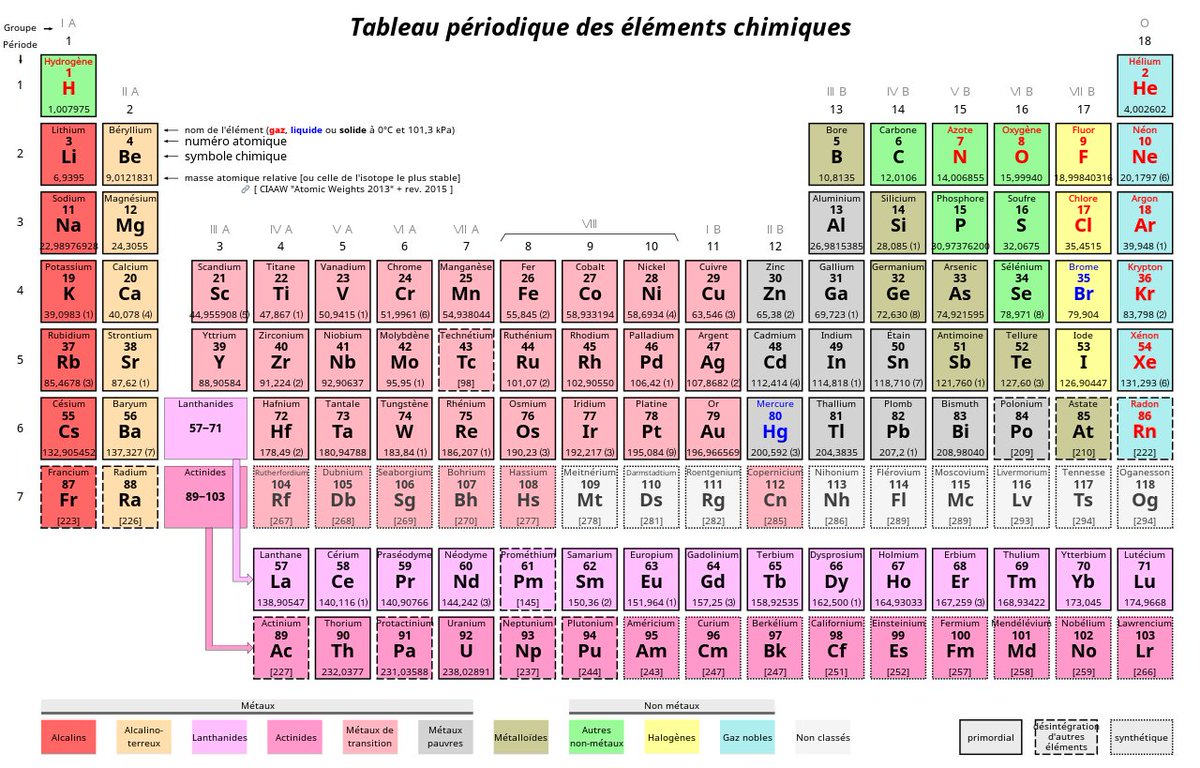
7️⃣ #Azote : N
Plus discret que le carbone mais pas moins essentiel pour la vie, l'azote est en fait bourré de contradictions.
Un formidable stimulant pour les uns, une arme de destruction pour les autres ; il est à la fois partout et invisible, inoffensif et dangereux 🤯
Plus discret que le carbone mais pas moins essentiel pour la vie, l'azote est en fait bourré de contradictions.
Un formidable stimulant pour les uns, une arme de destruction pour les autres ; il est à la fois partout et invisible, inoffensif et dangereux 🤯

L'apparent manque de cohérence entre son nom (azote) et son symbole (N) traduit déjà une histoire tumultueuse.
Le symbole vient du latin «nitrogenium», signifiant «qui génère du salpêtre», un sel d'azote connu depuis l'Antiquité.
Le terme nitrogène fut la première appellation.

Le symbole vient du latin «nitrogenium», signifiant «qui génère du salpêtre», un sel d'azote connu depuis l'Antiquité.
Le terme nitrogène fut la première appellation.


Jusqu'à ce que Lavoisier (encore lui) foute le bordel dans la nomenclature et décide de le nommer «azote» : terme composé de a- (privatif) et du radical grec ζωτ- («vivant»), le tout signifiant «privé de vie».
Car contrairement à l'oxygène qui permet la respiration, l'azote tue.
Car contrairement à l'oxygène qui permet la respiration, l'azote tue.

Enfin, l'azote ne tue pas directement, on en respire en permanence (sous forme de diazote N2) car il compose ~80% de l'air...
Mais il passe totalement inaperçu !
Raison pour laquelle il aura fallu attendre 1772 pour que Daniel Rutherford soit le 1er à l'identifier dans l'air.
Mais il passe totalement inaperçu !
Raison pour laquelle il aura fallu attendre 1772 pour que Daniel Rutherford soit le 1er à l'identifier dans l'air.

Pourquoi une telle abondance dans l'air ?
1) C'est un élément commun dans l'Univers
2) Sa forme moléculaire N2 est extrêmement stable : il faut une énergie considérable pour briser les 3 liaisons qui lient les 2 atomes d'azote
Ainsi, il est presque aussi inerte que l'hélium !
1) C'est un élément commun dans l'Univers
2) Sa forme moléculaire N2 est extrêmement stable : il faut une énergie considérable pour briser les 3 liaisons qui lient les 2 atomes d'azote
Ainsi, il est presque aussi inerte que l'hélium !

C'est pourquoi on l'utilise pour contrôler l'atmosphère de certains dispositifs : il est rajouté pour chasser et remplacer l'oxygène (élément réactif comme on le verra).
C'est un des gaz les moins chers du marché puisque abondant et relativement simple à extraire de l'air.
C'est un des gaz les moins chers du marché puisque abondant et relativement simple à extraire de l'air.

Alors que les plantes adorent l'azote, elles sont malheureusement bien incapables de le récupérer dans l'air (c'est con).
L'azote doit être contenu dans des formes biodisponibles pour être assimilés, d'où l'utilisation d'engrais à base de composés azotés (nitrate, ammonium...).
L'azote doit être contenu dans des formes biodisponibles pour être assimilés, d'où l'utilisation d'engrais à base de composés azotés (nitrate, ammonium...).
Même si les plantes n'ont pas attendu les engrais artificiels pour pousser, la production industrielle d'ammoniac NH3 (procédé Haber-Bosh) a été un tournant dans l'histoire :
N2 + 3H2 -> 2NH3
L'utilisation d'engrais de synthèse a réduit considérablement le risque de famines.
N2 + 3H2 -> 2NH3
L'utilisation d'engrais de synthèse a réduit considérablement le risque de famines.

Le souci, c'est que ce même ammoniac permet aussi de produire des explosifs ! 💥
TNT (trinitrotoluene), nitroglycérine, nitrate d'ammonium, 'y a comme une racine commune non ? 🤔
Ces composés azotés sont très réglementés, mais ça n'empêche pas certains méfaits ou accidents...
TNT (trinitrotoluene), nitroglycérine, nitrate d'ammonium, 'y a comme une racine commune non ? 🤔
Ces composés azotés sont très réglementés, mais ça n'empêche pas certains méfaits ou accidents...
L'explosion au port de Beirut en 2020 vient de plusieurs facteurs dont le mauvais entreposage d'engrais à base de nitrate d'ammonium !
[Instant auto-promo] Pour en comprendre les subtilités, allez voir la vidéo que j'avais faite sur le sujet :
[Instant auto-promo] Pour en comprendre les subtilités, allez voir la vidéo que j'avais faite sur le sujet :
Pour revenir sur un sujet moins chaud, le diazote est souvent préféré dans sa forme liquide car il se trouve alors à -196ºC, une température idéale pour éclater des verrues, conserver des aliments ou refroidir des composants électroniques de nombreux instruments scientifiques !
Enfin, on n'oublie pas le protoxyde d'azote (N2O) pour ses côtés anesthésiant et «hilarant» : sa vente est interdite aux mineurs depuis 2021 pour limiter son usage récréatif tournant parfois à l'asphyxie.
C'est aussi un des plus puissants gaz à effet de serre anthropogéniques.
C'est aussi un des plus puissants gaz à effet de serre anthropogéniques.
Pour résumer :
Chauffant et refroidissant, parfois mortel et pourtant vital, l'azote est impliqué dans tout et son contraire.
Tirant ses applications de l'hélium et son importance biologique du carbone, c'est un hybride qu'on retrouve partout mais souvent eclypsé devant C et O.
Chauffant et refroidissant, parfois mortel et pourtant vital, l'azote est impliqué dans tout et son contraire.
Tirant ses applications de l'hélium et son importance biologique du carbone, c'est un hybride qu'on retrouve partout mais souvent eclypsé devant C et O.
• • •
Missing some Tweet in this thread? You can try to
force a refresh