177/365
A veces, los químicos ha tratado de dirigir sus rutas de síntesis por los caminos que ha trazado la evolución biológica. En 1987 se otorgó el premio Nobel de Química “por el desarrollo y uso de moléculas con interacciones específicas de estructura de alta selectividad”.
A veces, los químicos ha tratado de dirigir sus rutas de síntesis por los caminos que ha trazado la evolución biológica. En 1987 se otorgó el premio Nobel de Química “por el desarrollo y uso de moléculas con interacciones específicas de estructura de alta selectividad”.
Donald J. Cram de la Universidad de California en LA, Jean-Marie Lehn de la Universidad Luis Pasteur en Estrasburgo, Francia y Charles J. Pedersen de DuPont de Nemours & Co. recibieron el Nobel por sus trabajos sobre el reconocimiento molecular en las reacciones enzimáticas. 

Charles J. Pedersen, de DuPont, con la síntesis de grandes compuestos cíclicos, formados por cadenas de carbono que a intervalos regulares tienen un átomo de oxígeno (los llamó éteres corona) inició las investigaciones que llevaron al descubrimiento de los criptandos, en 1967. 

Los éteres corona cíclicos tienen afinidad por iones de metales alcalinos a los que alberga en su centro, en ausencia de estos iones perdían su estructura organizada, parecida a un plato. Jean-Marie Lehn también los estudió desde el punto de vista 3D. 



Lehn estudió a los éteres corona cíclicos agregando capas de ellos, lo cual los hacía similares a platos apilados. Así fue como logró compuestos policíclicos a los que llamó criptandos por contener un orificio central o cripta (del griego kryptos, que significa “escondido”). 


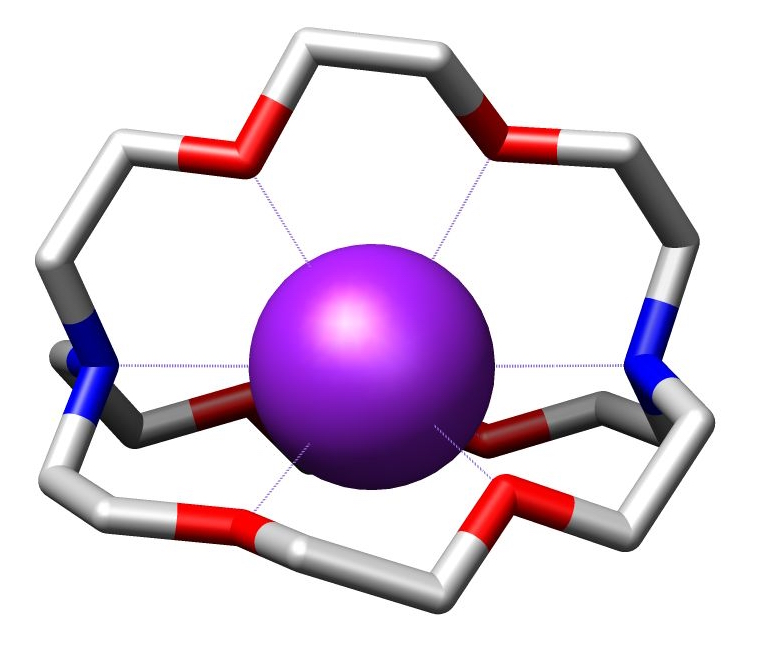
Los estudios cristalográficos permitieron apreciar que la unión del criptando con su substrato siempre producía modificaciones altamente transitorias en ambas moléculas, debido a que retornaban a su estado normal en fracción de segundos al dejar de interactuar. 

Cuando los complejos de Lehn aceptaban una molécula central, ésta era acoplada de manera muy específica, de forma tal que pareciera que se acomodaban. A diferencia de la mayoría de las reacciones en la química orgánica no se formaban enlaces covalentes sino débiles interacciones 

electrostáticas lo cual explica la transitoriedad de las reacciones criptando-substrato. Lehn llamó a esta fenomenología: Química supramolecular convencido de q en la química d este tipo d macromoléculas se presentan situaciones y problemas diferentes que entre moléculas pequeñas
Los éteres corona y los criptandos son ejemplos de los llamados ionóforos, sistemas capaces de transportar iones. Secuestran (enmascarar) a los iones metálicos en el interior d una estructura con superficie hidrofóbica (el esqueleto hidrocarbonado) soluble en disolventes apolares
Tuit 177 con información de:
K. E. Krakowiak, J. S. Bradshaw, H.-Y. An and R. M. Izatt (1993). «Simple methods for the preparation of cryptands». Pure Appl. Chem. 65 (3): 511-514. doi:10.1351/pac199365030511
K. E. Krakowiak, J. S. Bradshaw, H.-Y. An and R. M. Izatt (1993). «Simple methods for the preparation of cryptands». Pure Appl. Chem. 65 (3): 511-514. doi:10.1351/pac199365030511

• • •
Missing some Tweet in this thread? You can try to
force a refresh