Wissenschaftler entdecken Rezeptor, der #COVID19-Infektion blockiert
Wissenschaftler der Universität Sydney haben ein Protein in der Lunge entdeckt, das eine #SARSCoV2-Infektion verhindert und eine natürliche Schutzbarriere im menschlichen Körper bildet.
#Coronavirus #LongCovid
Wissenschaftler der Universität Sydney haben ein Protein in der Lunge entdeckt, das eine #SARSCoV2-Infektion verhindert und eine natürliche Schutzbarriere im menschlichen Körper bildet.
#Coronavirus #LongCovid

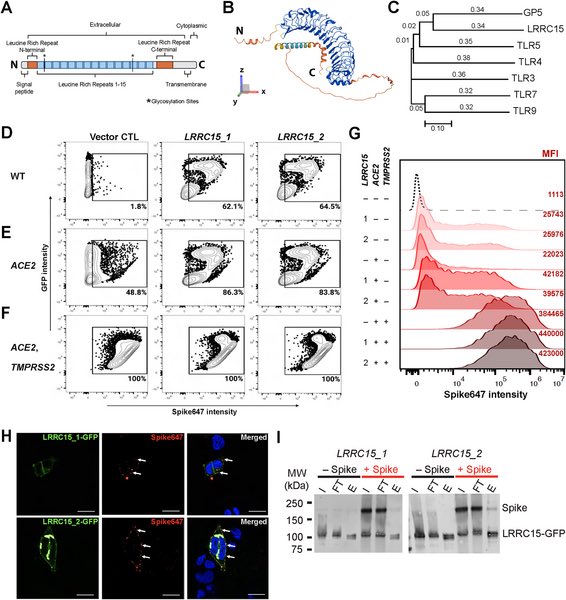
Dieses Protein, das leucine-rich repeat-containing protein 15 (LRRC15), ist ein eingebauter Rezeptor, der das SARS-CoV-2-Virus bindet, ohne die Infektion weiterzugeben.
Die Forschungsarbeit eröffnet einen völlig neuen Bereich der immunologischen Forschung rund um LRRC15 und
Die Forschungsarbeit eröffnet einen völlig neuen Bereich der immunologischen Forschung rund um LRRC15 und

bietet einen vielversprechenden Weg zur Entwicklung neuer Medikamente zur Verhinderung von Virusinfektionen durch Coronaviren wie COVID-19 oder zur Behandlung von Fibrose in der Lunge.
Die Studie der Universität ist eine von drei unabhängigen Arbeiten, die die Interaktion dieses
Die Studie der Universität ist eine von drei unabhängigen Arbeiten, die die Interaktion dieses
spezifischen Proteins mit COVID-19 aufzeigen und wurde von Professor Greg Neely und seinen Mitarbeitern Dr. Lipin Loo und Matthew Waller geleitet. Zusammen mit zwei anderen Gruppen, eine in Oxford, die andere in Brown und Yale in den USA, haben sie einen neuen Rezeptor im
LRRC15-Protein gefunden, der SARS-CoV-2 stoppen kann. „Wir fanden heraus, dass dieser neue Rezeptor an das Virus bindet und es sequestriert, was die Infektion reduziert", sagte Professor Neely. "Für mich als Immunologe ist die Tatsache, dass es diesen natürlichen Immunrezeptor
gibt, von dem wir nichts wussten, der unsere Lungen auskleidet und das Virus blockiert und kontrolliert, wahnsinnig interessant.
Wir können diesen neuen Rezeptor nun nutzen, um breit wirkende Medikamente zu entwickeln, die Virusinfektionen blockieren oder sogar Lungenfibrose
Wir können diesen neuen Rezeptor nun nutzen, um breit wirkende Medikamente zu entwickeln, die Virusinfektionen blockieren oder sogar Lungenfibrose
unterdrücken können." Das COVID-19-Virus infiziert den Menschen, indem es sich mithilfe eines Spike-Proteins an einen bestimmten Rezeptor in unseren Zellen anheftet. Es nutzt in erster Linie ein Protein namens Angiotensin-Converting Enzyme 2 (ACE2)-Rezeptor, um in menschliche
Zellen einzudringen. Lungenzellen weisen eine hohe Anzahl von ACE2-Rezeptoren auf, weshalb das COVID-19-Virus in diesem Organ infizierter Menschen häufig schwere Probleme verursacht.
Wie ACE2 ist auch LRRC15 ein Rezeptor für Coronaviren, d. h. das Virus kann sich an ihn binden.
Wie ACE2 ist auch LRRC15 ein Rezeptor für Coronaviren, d. h. das Virus kann sich an ihn binden.
Aber im Gegensatz zu ACE2 unterstützt LRRC15 die Infektion nicht. Es kann sich jedoch an das Virus heften und es unbeweglich machen. Auf diese Weise verhindert es, dass andere gefährdete Zellen infiziert werden. "Wir denken, dass es ein bisschen wie ein molekularer
Klettverschluss wirkt, indem es an der Spitze des Virus haftet und es dann von den Zielzelltypen wegzieht", so Dr. Loo.
„Im Grunde ist das Virus mit dem anderen Teil des Klettverschlusses umhüllt, und während es versucht, zum Hauptrezeptor zu gelangen, kann es sich in diesem Netz
„Im Grunde ist das Virus mit dem anderen Teil des Klettverschlusses umhüllt, und während es versucht, zum Hauptrezeptor zu gelangen, kann es sich in diesem Netz
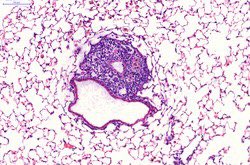
von LRRC15 verfangen", so Waller. LRRC15 ist an vielen Stellen zu finden, z. B. in der Lunge, der Haut, der Zunge, den Fibroblasten, der Plazenta und den Lymphknoten. Die Forscher fanden jedoch heraus, dass die menschliche Lunge nach einer Infektion mit LRRC15 aufleuchtet.
"Wenn wir die Lungen von gesundem Gewebe färben, sehen wir nicht viel LRRC15, aber in COVID-19-Lungen sehen wir viel mehr von dem Protein", sagte Dr. Loo. "Wir denken, dass dieses neu identifizierte Protein Teil der natürlichen Reaktion unseres Körpers auf die Bekämpfung der
Infektion sein könnte, indem es eine Barriere bildet, die das Virus physisch von unseren Lungenzellen trennt, die am empfindlichsten auf COVID-19 reagieren."
"Als wir die Funktionsweise dieses neuen Rezeptors untersuchten, stellten wir fest, dass dieser Rezeptor auch die
"Als wir die Funktionsweise dieses neuen Rezeptors untersuchten, stellten wir fest, dass dieser Rezeptor auch die
antiviralen Reaktionen sowie die Fibrose steuert und einen Zusammenhang zwischen der COVID-19-Infektion und der Lungenfibrose herstellen könnte, die bei Long COVID auftritt", sagte Waller. "Da dieser Rezeptor die COVID-19-Infektion blockieren und gleichzeitig die antivirale 
Reaktion unseres Körpers aktivieren und die Fibrose-Reaktion unseres Körpers unterdrücken kann, ist dies ein wirklich wichtiges neues Gen", sagte Professor Neely.
"Diese Entdeckung kann uns helfen, neue antivirale und antifibrotische Medikamente zu entwickeln, um pathogene
"Diese Entdeckung kann uns helfen, neue antivirale und antifibrotische Medikamente zu entwickeln, um pathogene
Coronaviren und möglicherweise auch andere Viren oder andere Situationen, in denen Lungenfibrose auftritt, zu behandeln. "Für Fibrose gibt es keine guten Medikamente: Die idiopathische Lungenfibrose beispielsweise ist derzeit unbehandelbar."
Fibrose ist eine Erkrankung, bei der
Fibrose ist eine Erkrankung, bei der
das Lungengewebe vernarbt und verdickt wird, was zu Atembeschwerden führt. COVID-19 kann Entzündungen und Schäden in der Lunge verursachen, die zu Fibrose führen.
Die Autoren erklärten, dass sie mit Hilfe von LRRC15 zwei Strategien gegen COVID-19 entwickeln, die bei mehreren
Die Autoren erklärten, dass sie mit Hilfe von LRRC15 zwei Strategien gegen COVID-19 entwickeln, die bei mehreren
Varianten funktionieren könnten - eine, die auf die Nase als vorbeugende Behandlung abzielt, und eine andere, die auf die Lunge für schwere Fälle abzielt. Die Forscher sagten auch, dass das Vorhandensein oder Fehlen von LRRC15, das an der Lungenreparatur beteiligt ist, ein
wichtiger Hinweis darauf ist, wie schwer eine COVID-19-Infektion werden könnte.
"Eine Gruppe am Imperial College London hat unabhängig davon festgestellt, dass das Fehlen von LRRC15 im Blut mit einer schwereren COVID-Infektion einhergeht, was unsere Vermutung bestätigt. Dr. Loo
"Eine Gruppe am Imperial College London hat unabhängig davon festgestellt, dass das Fehlen von LRRC15 im Blut mit einer schwereren COVID-Infektion einhergeht, was unsere Vermutung bestätigt. Dr. Loo
sagte. "Wenn Sie weniger von diesem Protein haben, haben Sie wahrscheinlich eine schwere COVID-Erkrankung, wenn Sie mehr davon haben, ist Ihre COVID-Erkrankung weniger schwerwiegend. "Wir versuchen nun zu verstehen, warum dies der Fall ist.
Im Rahmen der Forschung wurden
Im Rahmen der Forschung wurden
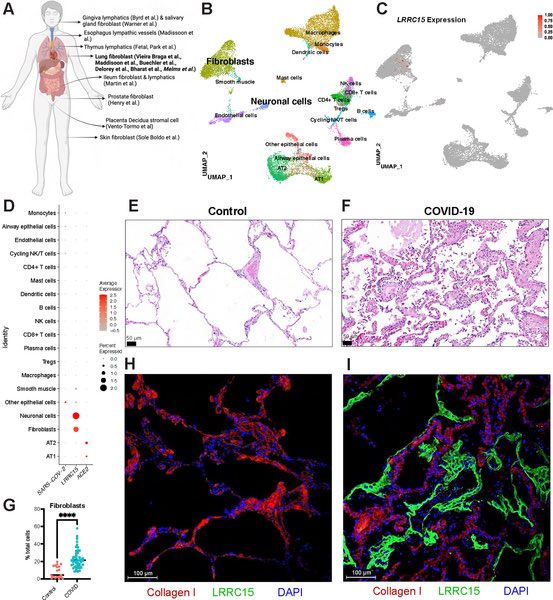
menschliche Zellkulturen nach Genen durchsucht und die Lungen von #COVID19-Patienten untersucht.
Die Links zu Bericht und Studien:
sydney.edu.au/news-opinion/n…
journals.plos.org/plosbiology/ar…
biorxiv.org/content/10.110…
biorxiv.org/content/10.110…
#Coronavirus #LongCovid #SARSCoV2
Die Links zu Bericht und Studien:
sydney.edu.au/news-opinion/n…
journals.plos.org/plosbiology/ar…
biorxiv.org/content/10.110…
biorxiv.org/content/10.110…
#Coronavirus #LongCovid #SARSCoV2
• • •
Missing some Tweet in this thread? You can try to
force a refresh