What makes kids so remarkably resilient to acute #COVID19 as compared to grownups and, especially, the elderly?
Here we take a deep (#singlecell) look into their noses and follow up on what we found in a cell culture model.
#SARSCoV2 #innateimmunity #children #adults
🧵1/15
Here we take a deep (#singlecell) look into their noses and follow up on what we found in a cell culture model.
#SARSCoV2 #innateimmunity #children #adults
🧵1/15
https://twitter.com/emboreports/status/1713996021137608783
Colleagues at BIH @berlinnovation @ChariteBerlin have previously collected nasal swabs of children and adults in the context of #SARSCoV2 and performed single cell transcriptomics #scRNASeq. We described a baffling #interferon response in children:
2/15
2/15
https://x.com/TheBinderLab/status/1428000748231593989?s=20
We now followed up on these findings wondering what causes the nasal epithelium of kids to be so much more sensitive to detect virus #infection. We reused the #scRNA data focussing specifically on healthy, uninfected individuals, and we combined it with in vitro experiments.
3/
3/
Kids epithelial cells were in a „primed state“, similar to cells exposed to type I #IFN, already in the absence of infection. Would that explain why they respond so much better to #SARSCoV2 infection than adults? Our A549 cell culture model says: yes!
4/15
4/15
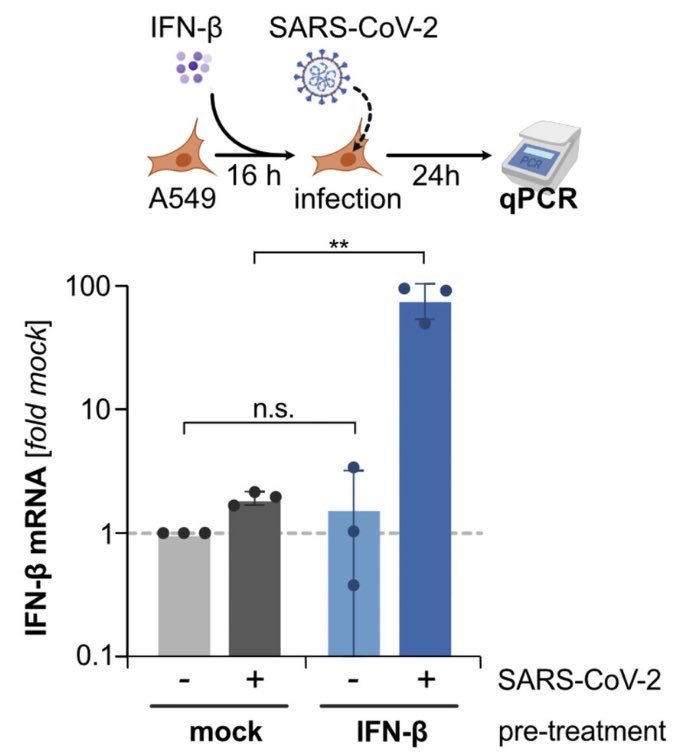
A basic but often overlooked effect: paracrine IFN strongly sensitizes the antiviral sensing system of cells– responses get stronger and (important!) much swifter! This is largely due to upregulation of sensors like RIG-I & MDA5. And this is also what we find in children.
5/15



5/15



OK, so it seems to be a constitutive priming of epithelial cells going on in kids but not in adults that makes them so sensitive, enabling timely sensing of #SARSCoV2 and a strong IFN response. But why would kids have constitutive levels of type I IFN in their mucosa?
6/15
6/15
The singe cell data revealed that kids have way higher amounts of immune cells in their nasal mucosa. More importantly, though, these immune cells are also more „active“, engaging in many more interactions with the epithelial cells! Does this prime epithelial cells?
7/15
7/15

Most likely: yes! Most immune->epithelial interactions are mediated by cytokines. When we tickle immune cells (PBMCs) in vitro and put their supernatants on A549, we indeed see upregulation of RIG-I and MDA5, much akin to our IFN-b pre-treatment above (tweets 4&5).
8/15
8/15

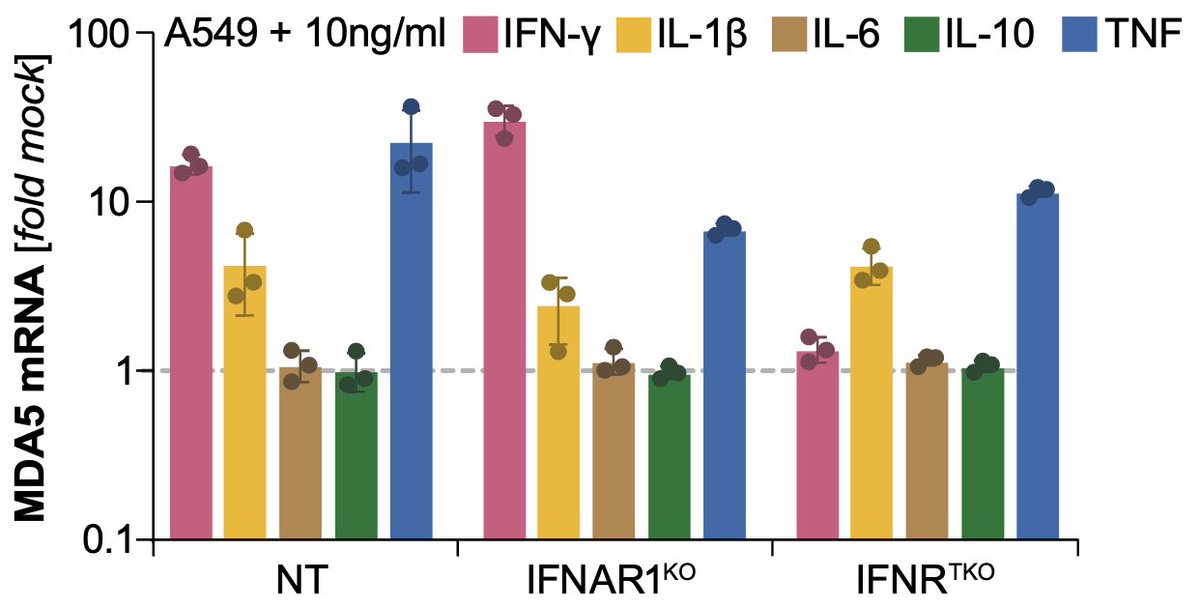
While in vitro supernatants contained IFN-a, immune cells from nasal swabs didn’t, but several of the other cytokines were indeed expressed. Particularly in kids we found the pro-inflammatory IFN-gamma and TNF. Can they, too, trigger RIG-I/MDA5 expression in epithelial cells?
9/
9/

Actually they can! Surprisingly, for TNF this was in fact completely independent of IFN signaling (TNF can indirectly trigger STING signaling) but strongly dependent on IRF1! We found TNF pre-treatment can sensitize cells similarly to IFN-b (see above), by inducing RLRs:
10/15



10/15


So are kids just more exposed to microbes and therefore regularly produce cytokines? Or are immune cells of kids inherently more active? For sure kids are less hygienic, but on top, we found their immune cells also tend to produce more cytokines to the very same stimulus!
11/15


11/15


This appears to be the inverse of #immunosenescence– while innate immunity gets slower in the elderly, kids have a particularly strong and active innate immune system. This makes alot sense, actually, as they haven’t trained their adaptive system yet, lacking immune memory.
12/
12/
To compensate for this lack of ready-made antibodies and T-cells, kids rely much more on a swift and strong innate immune response. Check out this great review by Peter Palese @IcahnMountSinai, to which our findings fit perfectly:
13/15nature.com/articles/ni1530
13/15nature.com/articles/ni1530
I want to also highlight this beautiful study by Julius Beer, @MartinSchwemmle and Daniel Schnepf @sandpiper_89. They asked the inverse question to ours: why are elderly individuals (mice in their case) more susceptible to COVID than mid-aged adults.
14/
14/
https://x.com/sandpiper_89/status/1572963581653839872?s=20
Surprise, surprise: aged mice produce less IFN-gamma! Exactly one of the cytokines we found to be enriched in children’s noses and to strongly prime the antiviral response of epithelial cells! Giving IFN-gamma to aged mice restores their antiviral response!
15/15
15/15

Lastly, let me thank everyone involved in our study: the almighty first author @VladimirMagalh, with some help by @DrechslerMaike, Sandra Wüst and @Sandy_Niesik. ScRNASeq analysis by Sören Lukassen and @jennyloske from @CaptainSysBio and Irina Lehmann @berlinnovation.
PBMCs of kids and adults were contributed by Aleš Janda and Eva-Maria Jacobsen from K.-M. Debatin’s clinic @UniklinikUlm, and Stella Autenrieth. Jobst Röhmel and Marcus Mall @ChariteBerlin (and #DZL) were key for the original sampling of nasal swabs.
And lastly, I really want to thank the @dkfz for supporting #SARSCoV2 / #COVID19 research through the fightCOVID@dkfz initiative!
If you understand German, you can read the DKFZ press release on the paper here: dkfz.de/de/presse/pres…
If you understand German, you can read the DKFZ press release on the paper here: dkfz.de/de/presse/pres…
@DKFZ Ah, just saw it’s available in English as well: dkfz.de/en/presse/pres…
@DKFZ @threadreaderapp unroll
(I will then link the generated unrolled thread on my mirror accounts on Mastodon and Bluesky)
(I will then link the generated unrolled thread on my mirror accounts on Mastodon and Bluesky)
• • •
Missing some Tweet in this thread? You can try to
force a refresh

 Read on Twitter
Read on Twitter